Чем наc лечат: Авифавир
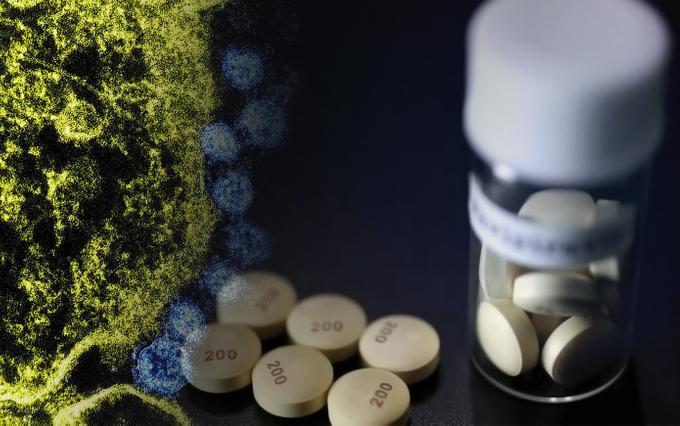
Быстрый, противовирусный, твой
Что за молекула стоит за первым в мире специфическим препаратом от коронавируса, якобы разработанным в России, какие трудности перевода испытывают РНК-вирусы внутри клетки и можно ли верить заявлениям в СМИ в отсутствие научных публикаций в рецензируемых журналах, разбираемся в новом выпуске рубрики «Чем нас лечат».
В отечественные клиники завозят первый зарегистрированный в России препарат от коронавируса — Авифавир. Он считается первым в мире официально зарегистрированным лекарством по этому показанию. Хотя говорилось о начавшихся испытаниях и в других странах, Россия опередила всех, выдав разрешение на использование препарата. Теперь Авифавир можно будет получить по ОМС бесплатно, и поставки первых партий уже организованы в 35 российских регионов. Но не слишком ли быстро сделаны эти выводы?
Новый препарат вызвал переполох в научной среде. Упомянула его в брифинге и главный исполнительный директор Всемирной организации здравоохранения Сумия Шваминатан, которая признается, что следит за его исследованиями с интересом и «будет рада посмотреть на результаты».
Настораживает, что результатов исследований производители еще не опубликовали в научной литературе: нет их ни в русскоязычной базе научных статей КиберЛенинка, ни в PubMed. Но как же так? Ведь без исследований на людях зарегистрировать препарат невозможно. Несмотря на то что в условиях пандемии агентства по всему миру принялись экстренно упрощать процедуры регистрации препаратов и клинических испытаний, обойтись без них нельзя. Однако информация на сайте российского Госреестра лекарственных средств подтверждает — препарат получил разрешение 29 мая. Распространяться будет лекарство в пачках и флаконах по 10 или 40 таблеток.
Значит ли это, что отныне Авифавир можно купить в аптеках? Нет, это не так. Ускоренная регистрация стала возможна только с четырьмя условиями(помимо письменного согласия каждого пациента):
- — лечить пациентов Авифавиром от коронавирусной инфекции можно только в стационаре;
- — препарат выпускается под обязательным посерийным контролем качества;
- — Федеральная служба по надзору в сфере здравоохранения ведет учет каждого применения этого лекарства;
- — Минздрав все еще ждет отчета о клиническом испытании по протоколу № COVID-19-FPR-01.
Это адаптивное многоцентровое рандомизированное сравнительное клиническое исследование ООО «Кромис», которое проводится совместными усилиями 35 медицинских организаций на 390 пациентах, госпитализированных с COVID-19. Окончить испытание планируется 31 декабря 2020 года, но разработчики и вложившийся в препарат Российский фонд прямых инвестиций уже вовсю рассказывают СМИ о результатах.
Согласно их заявлениям, 65% пациентов из 40 человек, принимавших Авифавир, получили отрицательный тест на коронавирус уже через четыре дня, «что в два раза выше, чем в группе стандартной терапии». На десятый день 90% пациентов в группе Авифавира получили отрицательный результат. У 68% из этой же группы температура тела вернулась в норму на третий день, тогда как у группы контроля, которой препарат не давали, температура держалась в среднем в два раза дольше. Увы, более подробной информации авторы не предоставляют. Мы не знаем, ни сколько раз делали тест (чтобы уменьшить процент ложноотрицательных результатов), ни других подробностей. «Авторы говорят про то, что включили в исследование контрольную группу, но тут возникают вопросы, что за пациенты вошли в нее, какова была тяжесть течения заболевания и какое лечение они получали», — указывает на еще одно несоответствие заместитель исполнительного директора по медицинскому направлению BestDoctor Юлия Ткаченко.
Справка |
Тот же дедлайн, 31 декабря 2020 года, установлен и для исследования фавипиравира компанией «Промомед Рус», которая разрабатывает его под брендом Арепливир, только пациентов в испытании поучаствует 210, а медицинских центров — 5. На год позже окончит испытания компания «Технология лекарств» (кстати, по адресу почти идентичная «Кромис», разница лишь в номере строения). Они проверят действие препарата на пациентах с легкой и среднетяжелой формой заболевания.
Все эти испытания относятся к третьей фазе, которая в норме предшествует регистрации препарата. Несмотря на рандомизацию, группу сравнения и разные медицинские центры, три исследования остались открытыми, то есть без ослепления. А значит, их итоги легко могут быть искажены субъективностью или даже намеренным жонглированием статистикой.
Справка |
Вопросы к числам
На этом путаница только начинается. В интервью с заведующим приемным отделением Медицинского научно-образовательного центра МГУ им. Ломоносова Антоном Потапенко, к примеру, в начале говорится о 30 пациентах-участниках из их клиники, затем — о 48 (возможно, речь идет о разных фазах испытаний): «В мае было включено в исследование около 30 пациентов, которые принимали данный препарат и достаточно легко проходили лечение, достаточно быстро выписывались. […] У пациентов меньше развивалось различных осложнений, характерных для коронавируса: это массивное поражение легких, цитокиновый шторм не развивался. Из 48 пациентов, которые наблюдались у нас по данной программе, только один, к сожалению, попал в реанимацию с развитием дыхательной недостаточности. Но это был пациент достаточно пожилой, с большим количеством различных сопутствующих патологий».
Другие СМИ сообщают, что эти результаты были получены на 60 добровольцах, 20 из которых получали Амифавир в дозировке, рекомендованной Минздравом, а остальные 40 — в других. Подобное исследование помогает лишь подобрать безопасную дозировку для таблеток (при регистрации в таблетке указано 200 мг действующего вещества), но не доказывает их эффективность. Кроме того, такие проверки происходят на второй фазе испытаний, а в регистрационных документах указана третья. И судя по всему, речь все еще идет об испытании по протоколу № COVID-19-FPR-01, и в описание его дизайна это ясности не вносит (тем более что из-за спешки во время пандемии испытания разных фаз могут идти одновременно и параллельно). В любом случае, по стандартам доказательной медицины для оценки побочных эффектов даже вторая фаза должна была проводиться на нескольких сотнях пациентов, а мы пока видим гораздо меньше.
Интересно, что в Госреестре есть и более раннее двойное слепое испытание на 168 пациентах в 14 медицинских организациях, в котором препарат сравнивался с плацебо в борьбе против гриппа. И завершилось оно в 2015 году, хотя как препарат от гриппа его в России так и не одобрили. Только называется это вещество уже фавипиравир. Но одно ли это и то же? И если да, то как же быть с «российской разработкой» и на что получили грант ученые от Фонда «Сколково»?
Из чего же, из чего
Химическое наименование фавипиравира — 6-фтор-3-гидрокси-2-пиразинкарбоксамид. И именно фавипиравир назван в официальных источниках действующим веществом в составе Авифавира. Но ведь фавипиравир первыми одобрили японцы, а не русские, и не против коронавируса, а против гриппа, если более изученные римантадин, осельтамивир и занамивир не помогают. Лекарство с 2014 года продается в Поднебесной под маркой Авиган, а действие патента для него истекло в прошлом году.
Но в чем тогда вклад российской компании «Кромис», выполнявшей исследования на деньги Фонда «Сколково»? Они предложили свою схему синтеза молекулы под названием 6-фтор-3-гидрокси-2-пиразинкарбоксамид и провели доклинические испытания (а теперь проводят клинические). ТАСС тут же назвал молекулу «российской», хотя химически это тот же самый японский фавипиравир. Другие СМИ ничтоже сумняшеся окрестили его «первым отечественным препаратом от коронавируса», хотя действительности это не соответствует.
Структура фавипиравира Ben Mills/Wikimedia Commions
Каков же предполагаемый механизм действия фавипиравира? В организме человека он изменяется, превращаясь в фавипиравир-рибофуразил-5’-трифосфат. Предположительно, такой «багаж опыта» ему прибавляет человеческий фермент гипоксантин-гуанинфосфорибозилтрансфераза, или ГГФТ.
ГГФТ участвует в синтезе некоторых из «кирпичиков», входящих в состав ДНК 1BZY/Wikimedia Commons
По задумке создателей, фавипиравир должен подавлять механизм размножения вирусов. Поскольку вирусы не могут сами воспроизводить себя, они порабощают для этого живые клетки. Однако РНК-вирусы (в том числе грипп, коронавирус и вирус Эболы) записывают и хранят свои данные по сборке новых молекул белка не в виде ДНК, как мы с вами, а в виде РНК, которую наши клетки используют совсем для другого. Таким вирусам приходится несколько раз переписывать генетическую информацию, приводя ее в тот вид, в котором захваченная клетка «поняла» бы их приказы. Производное препарата, фавипиравир-рибофуразил-5’-трифосфат, блокирует работу фермента РНК-зависимой РНК-полимеразы, которая помогает РНК-вирусам «перевести» свою генетическую информацию. По другой версии, фавипиравир заставляет вирусы мутировать в нежизнеспособную форму.
Эти механизмы удалось продемонстрировать на клеточных культурах легких морских свинок и даже людей, на клетках собачьих почек и других моделях in vitro (что значит «в пробирке»), но неясно, какой из них работает на животных. Известно лишь, что синтезу РНК и ДНК в клетках млекопитающих он не мешает. Кроме гриппа, на животных он показал активность против ряда других вирусных заболеваний — Эболы, лихорадки Западного Нила, вируса Зика и даже против бешенства.
Но результаты плохо подтверждались на людях: так, в исследовании фавипиравира в борьбе с вирусом Эболы группой контроля стали предыдущие записи, а тяжело больным пациентам с самой высокой концентрацией частиц вируса в крови лекарство уже не помогло.
С гриппом успехи тоже были небольшие. Несмотря на пройденные испытания безопасности лекарства и доказательство того, что оно за 6-14 часов угнетает размножение вируса гриппа даже в детях с неработающим иммунитетом после трансплантации костного мозга, ни США, ни Великобритания фавипиравир против гриппа так и не одобрили. Зато это сделали Япония (в 2014) и Китай (в 2020).
В борьбе с коронавирусом в других странах завершены лишь предварительные исследования (как эта маленькая по масштабам работа в Китае), но в большинстве случаев они еще идут, и результат неизвестен. Так, итальянские эксперты здравоохранения еще недавно предупреждали: делать выводы по препарату преждевременно.
Тем не менее уже известно, что препарат вызывает побочные эффекты. Есть данные, предполагающие, что препарат опасен для развития плода. Кроме того, пока остаются открытыми вопросы про его влияние на работу сердца и кроветворение, а также про его возможную связь с раком. Возможно, он безопасен только для кратковременного применения.
Вывод можно сделать такой: «первый отечественный препарат от коронавируса» оказался не отечественным и не от коронавируса, а если рассматривать его как противовирусное средство в целом, то и не первым. По крайней мере, таким его создали изначально. По сути, препарат стал дженериком японского лекарства от тяжелых форм гриппа, которое и в первой своей ипостаси не очень-то оправдало ожидания. Оно пробовало свои силы в борьбе с разными эпидемиями, но пока что верх нигде не одержало. При этом в России был разработан новый метод его синтеза, и было бы неплохо сравнить, не хуже ли наш фавипиравир (Авифавир), чем японский (Авиган).
Однако препарат был изучен чуть больше по своим изначальным показаниям, и у него есть уже известные побочные эффекты. Возможно, он лучше гидроксихлорохина — в отличие от него, Авифавир, скорее всего, не влияет на QT-интервал (даже в дозе 12 таблеток). Также известно, что новый препарат не мешает работе парацетамола.
Результаты исследований, которые подтверждали бы эффективность Авифавира против коронавируса, не опубликованы в рецензируемых научных журналах, а лишь звучат в интервью, сопровождаемые красивыми цифрами «эффективность 90%». Несмотря на то что коронавирус торопит медиков по всему миру, а количество смертей убеждает в необходимости разрабатывать и утверждать новые лекарства как можно скорее, такое решение Минздрава следовало бы считать поспешным. Остается лишь надеяться, что отчеты об испытаниях, предоставленные в ведомство, вызывают доверие у специалистов. С другой стороны, прием препарата останется под строгим контролем врачей в стационаре, поэтому нанести много вреда он, вероятно, и не сможет.
Тем не менее осторожность не помешает, ведь возможны довольно серьезные побочные реакции, например различные нарушения производства клеток крови, обмена глюкозы, калия, нитриглицерида и мочевой кислоты. Взаимодействует он и с другими лекарствами. Так, Авифавир усиливает эффект Пиразинамида и Репаглинида, подавляет работу Фамцикловира и Сулиндака, а его собственная концентрация в крови может возрасти от приема Теофиллина, что тоже нужно иметь в виду.
Наши рекомендации нельзя приравнивать к назначению врача. Перед тем, как начать принимать тот или иной препарат, обязательно посоветуйтесь со специалистом.
Источник: «Indicator»
- Политика
 С.С.Сулакшин Самое интересное
С.С.Сулакшин Самое интересноеПодпиши петицию: С.Сулакшин: «Президент Путин, дай России шанс развиваться, уйди в добровольную отставку!»
Степан Сулакшин создал(а) эту петицию, адресованную Путин, Народ России Устройство всех сфер жизни страны, политический режим в стране, его практики управления государством и результаты губительны для России и ее народа. За 20 лет путинизма все стало предельно ясно и безнадежно. Народ вымирает, падает рождаемость и растет смертность. Лучшая часть населения эмигрирует. Экономика деградирует в сырьевую…4 347 - Политика
 Русранд Сулакшин С.С.
Русранд Сулакшин С.С.Антироссийский проект путинизма: реконструкция, идеологические и фактические характеристики
Занимаемся мы в университете оппозиции не пропагандой, не агитацией (что только в какой-то мере так, но главная цель не в этом). Занимаемся мы тем, что убеждаем друг друга и помогаем понять, что слово «оппозиция» — слово ответственное и оно отличается от слов: «балаган», «развлекуха», «подставуха», «суррогат», самопиар и «политическая порнография». Мы делаем совершенно иную заявку и последовательно помогаем строить в стране настоящую политическую оппозицию. Правящий режим и правящая группировка в нашей стране, как известно, получила…981 - Экономика
 Русранд Самое интересное Степан Степанович Сулакшин
Русранд Самое интересное Степан Степанович СулакшинПутинизм и кризис России
Россия вновь наступает на те же грабли. Годы назад, выдвинув математическую модель мирового финансового кризиса, наша научная политическая группировка предупреждала руководство страны, что оно создает модель экономики и государства несуверенного типа, уязвимые для внешнего агрессивного воздействия. Обстоятельный доклад на эту тему в феврале 2009 году — по кризису одов — был подготовлен для Совета Безопасности Российской Федерации, в котором тогда, совместно с его секретарем Николаем…1 348 - Политика
 Русранд Самое интересное Степан Степанович Сулакшин
Русранд Самое интересное Степан Степанович СулакшинПОБЕДИТЬ МОЖЕТ ТОЛЬКО УМНАЯ ОППОЗИЦИЯ — Университет оппозиции. Выпуск №33
2 апреля в 20:00 мск очередной прямой эфир Университета оппозиции. Канал ютуб Центра Сулакшина. Присоединяйтесь. Политическая оппозиция обязана быть умной и просвещенной,только тогда возможна ее победа и оздоровление нашего Отечества! Тема выпуска: ПОБЕДИТЬ МОЖЕТ ТОЛЬКО УМНАЯ ОППОЗИЦИЯ Ведущий: Степан Степанович Сулакшин548 - Политика
 Сулакшин С.С.
Сулакшин С.С.Вступай в борьбу за власть
Уважаемый соотечественник! Благодарим вас за возможную решимость присоединиться к организационно-политическому строительству объединения настоящей общенародной оппозиции Путину и путинизму в рамках организационной инфраструктуры Партии Нового Типа. Наш отличительный принцип состоит в том, что мы не только разоблачаем губительный характер путинизма, но дали профессиональную диагностику способов и причин деградации страны и народа. В ее основе научные методы, модели и методология. Мы не только критикуем путинизм, но мы делаем настоящее профессиональное, конкретное содержательное предложение — что и как…716 - Политика
 Русранд
РусрандРоссии нужна другая Конституция!
Конституция — это основной закон страны. Существуют Конституции двух типов — первый, к которому относится ельцинско-путинская Конституция, устанавливает право, порядок и институты государственности. В Конституции иного типа кроме права, порядка и институтов задаются основы жизнеустройства во всех сферах жизни. Задаются социальная, экономическая, политическая, гуманитарная модель страны. Новая Конституция команды Сулакшина — именно такого, второго типа. Каким в Конституции будет задано жизнеустройство, — такой жизнь в стране и будет. Если…212 - Политика
 Русранд Самое интересное Степан Степанович Сулакшин
Русранд Самое интересное Степан Степанович СулакшинПутинизм должен исчезнуть! Вызовы оппозиции гибельному курсу России
Автор и его товарищи много усилий приложили для мобилизации в стране реальной политической оппозиции путинизму, но задача создания профессиональной оппозиции, способной взять на себя ответственность за страну, дело трудное, объемное и длительное. Ее решение только еще предстоит. Поэтому мы открыли Университет оппозиции. Это цикл публичных занятий, объединяющей темой которого является политический проект реальной оппозиции, ее политическая Программа. Простой на первый взгляд вопрос — да чего там, за вечер…172 - Общество
 Владимир Викторович Волк
Владимир Викторович ВолкЗачем плодить «новые социализмы», идя верной дорогой товарищей из системной КПРФ?
Пришла обратная реакция на публикацию «Профессор Сулакшин разобрал на молекулы «программу» Платошкина. Не соскучишься» . Кандидат экономических наук Анатолий Агафонов, в целом понимая, что Степан Сулакшин по делу и основательно разбил никчемную «программу-минимум» Николая Платошкина, возразил. Мол, у Николая Николаевича ещё всё спереди: вот он ознакомится с разбором Сулакшина, сделает выводы и придумает программу –максимум. А если…95
- Общество
 Русранд Степан Степанович Сулакшин
Русранд Степан Степанович СулакшинСемь «П». Программа: платформа, проблемная повестка, проект, план, прогноз
Центральная и сквозная тема наших занятий в Университете оппозиции — разбор политической программы — что это такое? Многим кажется, что политическая оппозиция, её роль, миссия и активная повестка демонстрируется в нашей стране, например, Левым фронтом Сергея Удальцова, активно организующего уличные акции; КПРФ с их митингами; был период, когда Навальный со своим политическим проектом будоражил страну множеством митингов по стране и несогласованными, и рискованными митингами в центре Москвы. То есть…13 - Общество
 Александр Берберов
Александр БерберовВова Зе и виртуальная реальность
Виртуальный мир «хорош» тем, что очень многие проблемы, присущие реальности, в нём не существуют. Свойственная реальности безусловность – сменяется в игре условиями игры, заданными заранее. И вот в этом условном, воображаемом мире, покорном фантазии заказчика, живут воображаемые, «цифровые» люди, реальные не больше, чем динозавры в фильмах о динозаврах. У этих людей воображаемые проблемы и воображаемые…20 - Общество
 Николай Выхин
Николай Выхин«Символ веры»: «чёрная либерагия» с разоблачением
Правильный подход, на мой взгляд – не выдумывать ничего за них, а просто цитировать их самих, они сами всё расскажут. И комментатора не упрекнут в натяжках и домысливании. Вот постоянный автор «Эха Москвы», депутат и либерал, более либеральный, чем Собчаки Борис Вишневский «…уверен в двух вещах. Первое: кто бы не выиграл, в США достаточно страховочных…20 - ОбществоEADaily
Жители Краматорска не пришли на премьеру фильма о победе Украины в войне
Кадры из фильма «Атлантида» напоминают постапокалипсис. Иллюстрация apostrophe.ua В городе Краматорске, который находится на подконтрольной Киеву части Донецкой области, сорвалась всеукраинская премьера фильма «Атлантида». Данный «киношедевр» относится к жанру фантастики (события в сюжете датируются 2025 годом) и рассказывает о том, что будет на Донбассе после того, как Украина победит в войне и вернет в свой состав территории ЛНР и ДНР. Стоит отметить, что этот фильм в сентябре по итогам…19 - Общество
 Канал «Центр Сулакшина»
Канал «Центр Сулакшина»ЧТО ТВОРИТСЯ В МЕДИНСТИТУТАХ РОССИИ? #Сулакшин #Эксперты АКТУАЛЬНЫЙ РАЗГОВОР ◄06.11.2020►
6 ноября в 20-00 МСК присоединяйтесь к актуальному разговору. Настоящее и будущее отечественной медицины — нас лечат или калечат? Кто виноват и что делать? Разговор с экспертами. Ведущий проф. С.С.Сулакшин. Тема выпуска: ЧТО ТВОРИТСЯ В МЕДИНСТИТУТАХ РОССИИ? Приходите на канал Центра Сулакшина в youtube. ПЕРЕЙТИ НА СТРАНИЦУ ПЕРЕДАЧИ21 - Общество
 Татьяна Бескаравайная
Татьяна БескаравайнаяПрофсоюзы спрогнозировали снижение выплат врачам за работу с коронавирусом
Отраслевые профсоюзы прогнозируют снижение размера доплат, получаемых медработниками за работу с пациентами с коронавирусом в рамках нового правительственного постановления. Выплаты могут вырасти только у тех, кто работает не на одну ставку и непосредственно в «красных зонах», уверяют их лидеры. ЦК профсоюза работников здравоохранения РФ подготовил запрос в Минтруда с просьбой разъяснить порядок начисления доплат в…18 - Общество
 Русранд
РусрандЗмей-искуситель и Андрейка
Публикуем замечательный рассказ Стебляковой Екатерины Григорьевны, великой труженицы, ребёнка войны, которая свято верила, что Россия обязательно очистится от зла. Давным-давно это было, люди уже многое позабыли. Так вот, на земле в ту пору народ дружный был, жили весело, не ссорились, кругом леса роскошные, в них зверья видимо-невидимо, реки чистые, вода в них хрустальная, а рыбы разной полным-полно. Поля просторные засевались хлебами, овощами, фрукты росли на каждом дереве, звери…22 - Общество
 Иван Захаров
Иван ЗахаровСын Цоя подал в суд на Алексея Учителя
Фото: кадр из х/ф «Игла», 1988 год. Реж. Р. Нугманов Сын Виктора Цоя Александр подал в суд на создателей фильма о своём отце. Исковое заявление музыканта зарегистрировано 5 ноября и находится у судьи, сообщили «Октагону» в Пресненском суде Москвы. Дело касается защиты права гражданина на изображение. Ответчиками выступают ООО «Каропрокат», ООО «СППР» и ООО ТПО «Рок». Киностудия…26 - Общество
 Канал «Центр Сулакшина»
Канал «Центр Сулакшина»Забытое право на счастье #ГолосНарода #ЛюбовьДонецкая
Автор Любовь Сергеевна Донецкая, Союз Народной Журналистики, команда поддержки Программы Сулакшина #ПрограммаСулакшина #СпастиРоссию #ПереустроитьРоссию #НравственноеГосударство #СулакшинПрав61 - Общество
 Русранд
РусрандПОЛИТИЧЕСКИЙ МОМЕНТ И ЗАДАЧИ ДВИЖЕНИЯ #ПрограммаСулакшина — ВСЕРОССИЙСКОЕ СОВЕЩАНИЕ МСК. Присоединяйся
В четверг 5 ноября 2020 в 18-00 МСК на ютуб-канале Центра Сулакшина принимайте участие онлайн-трансляции открытого Всероссийского рабочего совещания актива и сторонников Программы Сулакшина «Настоящий социализм». Реплики и вопросы задавайте в чате. #ПрограммаСулакшина ВСЕРОССИЙСКОЕ СОВЕЩАНИЕ46 - Общество
 Источник света
Источник светаПочему недовольным властью россиянам говорят, что у них всё есть, а им всё мало?
Фото отсюда: макарошки Часто от сторонников российской власти слышишь фразу: «народ зажрался, с жиру бесится, не знает своего счастья». Сама по себе фраза оскорбительная по отношению к людям. Но она и вопрос рождает: а чем народ зажрался-то? Творожным продуктом или тушенкой со шкурками? Молочкой и мясом с антибиотиками? Пальмовым маслом? Е-добавками? Ешь и думаешь: «авось…57 - ОбществоЕлена Петровская
Съедобное-несъедобное: чем должны кормить в школах и детских садах
©Дмитрий Рогулин/ ТАСС Пока на федеральном уровне обсуждается тема господдержки производителей питания для детских коллективов, в регионах происходят баталии по поводу проведения торгов, организуются мошеннические схемы сбора средств, а порой даже происходят пищевые отравления. Чиновники разрабатывают стандарты питания, но это зачастую совсем не то, что на самом деле любят и едят дети. Определиться со здоровым…27 - Обществоanlazz
О сути «исторического прогресса» в иллюстрациях
Для иллюстрации к описанной в прошлом посте ситуации с «научно-техническом прогрессом» и его реальных движущих силах очень хорошо подходит приводимый выше рисунок: Это — как написано — греческий герой Ясон пашет на быках. Ясон — если кто не знает — это тот «товарищ», который плавал в Кохиду за «Золотым Руном». С группой не менее авторитетных «товарищей» на…30 - Общество
 Редакция "Народного Журналиста"
Редакция "Народного Журналиста"Крым: нищета и ЗАПУСТЕНИЕ! Не верите? Посмотрите сами! Крымские степные села 1 часть.
Иерей Роман Колеснёв «Цель этого ролика: обратить внимание на жизнь людей в отдалённых сёлах (не только Крыма). Жизнь эта реальная и непридуманная. Никто не жалуется на жизнь, ни я, ни люди, которые там живут. Люди тянут каждый свою лямку. Просто о них все забыли, начиная от городских жителей и заканчивая власть имущими людьми. Я сам рад…4.11.2020 0:26 35 - Общество
 Сулакшин С.С.
Сулакшин С.С.#ПрограммаСулакшина Вопросы и ответы. Разговор с народом — Выпуск №84 ◄03.11.2020►
Степан Степанович отвечает на вопросы зрителей. С чего начинается познание мира и осознание себя в этом мире? Понимание своего положения и своего долга, решения на следующий шаг? С вопроса! Задай себе 1000 вопросов и заработает твоя мысль. Ты переберешь 1000 вариантов и найдешь ответ. В науке говорят — самое сложное это задать вопрос, поставить задачу. Задай свой вопрос на передачу «Страна станет другой! Вопросы и ответы» на канале Сулакшина…26 - Общество
 anlazz
anlazzОбразовательная катастрофа и развитие человечества. Часть вторая
Фото отсюда Первая часть тут . Я не буду разводить интригу относительно того, какое событие привело к изменению отношения к образованию – просто потому, что неоднократно о нем упоминал. Разумеется, речь идет о Великой Пролетарской Революции, начавшейся в 1917 году. Поскольку именно она привела к переоценке необходимости получения знаний массами. В том смысле, что получившие субъектность –…26 - Обществоanlazz
Образовательная катастрофа и развитие человечества. Часть первая
В прошлых постах (1, 2 , 3 ) – посвященных происходящему в настоящее время росту популярности т.н. «зеленых технологий» — было указано, что, в значительной мере, связано это с явлением, обозначенным, как «образовательная катастрофа». И хотя там же было кратко указано, в чем эта самая «катастрофа» состоит, однако есть смысл поговорить о данном явлении поподробнее. (Хотя я уже не…34 - Общество
 Анна Шахова
Анна ШаховаРасходы россиян упали до минимума с 2008 года
Расходы российских семей во втором квартале 2020 года упали на 12,8% год к году — до 16 490 рублей на члена семьи. С учётом инфляции это минимум с 2008 года. Такой вывод сделали аналитики международной сети FinExpertiza. Расходы россиян упали из-за снижения благосостояния и режима ограничений. Большинство россиян не смогли позволить себе прежний уровень потребления. Кроме того,…13 - Общество
 Афанасьев А.П.
Афанасьев А.П.Великая созерцательница
ПОТАЁННАЯ СИЛА ИНДИЙСКОГО НЕПРОТИВЛЕНЧЕСТВА Одно из древнейших государств мира — Индия продолжает ныне пребывать среди самых экзотических и загадочных стран современности. Одновременно её, наряду с Китаем, принято относить к одной из самых древних мировых цивилизаций, коими обычно считаются державы, достигшие высокого уровня общественного развития, материальной и духовной культуры. Неразгаданная в течение тысячелетий тайна и вполне доступная физическим ощущениям реальность — такой предстаёт перед нами Республика…45 - Общество
 Редакция "Народного Журналиста"
Редакция "Народного Журналиста"В Питере объявлена голодовка
В сети появилась петиция, где изложена суть проблемы. Люди в отчаянии. Требуем достроить ЖК «Три апельсина» и» На заречной» «Мы, обманутые дольщики строительной компании Норманн (ЖК Три Апельсина и ЖК На Заречной). Нас более 1800 семей, которые, с 2014 года ждут свои квартиры. Более половины семей платят ипотеки и с детьми. Среди дольщиков есть пенсионеры и инвалиды! В 2016…45 - Общество
 Марина Юршина
Марина ЮршинаДенег на выплаты больничных может не хватить
©Shutterstock/Fotodom Специалисты Счетной палаты выявили в бюджете Фонда социального страхования (ФСС) РФ дефицит средств, предусмотренных на выплату пособий по больничным и в связи с материнством. Уже сейчас в бюджете Фонда не хватает 31 млрд рублей для этих категорий застрахованных. Такая ситуация сложилась на фоне проводимой в отрасли реформы, а экономический кризис, вызванный пандемией коронавируса, еще…27 - Общество
 Александр Леонидов
Александр ЛеонидовБосяцкий рай и цивилизационное принудилово
Скажу очень научную фразу – только вы сразу не пугайтесь: животное начало в человеке тяготеет к постоянному снижению интенсивности физической и умственной деятельности при возрастающей их случайности, бессистемности. Заложенный в человеке инстинкт, когда пущен на самотёк, особенно смолоду – склонен, например, читать всё меньше, и при этом – всё более и более случайные тексты. Происходит…71 - ОбществоАнастасия Николаева
Доказать незаконность сделки
Фото сайта БСК Interfax-Russia.ru — Арбитражный суд Башкирии приступил к рассмотрению дела о приватизации «Башкирской содовой компании». Власти Башкирии считают, что компания была приватизирована незаконно, совладелец с этим утверждением не согласен. Судебное разбирательство инициировала Генпрокуратура РФ, которая 28 августа направила в канцелярию Арбитражного суда Башкирии иск о незаконности сделки, из-за которой государство утратило контроль над АО…31 - Общество
 Никита Пономаренко
Никита ПономаренкоЛед в Арктике не стал замерзать впервые в истории
Климатический кризис ускоряет таяние льда по всей Арктике. Нарушение цикла в море Лаптевых может повредить экосистемам в других регионах Северного Ледовитого океана. Никита Пономаренко, 22 октября 2020 Ученые в Университете штата Колорадо отметили, что впервые в истории наблюдений море Лаптевых остается безо льда к концу октября. Климатический кризис приводит к тому, что Арктика нагревается в 2-3 раза быстрее,…50 - Общество
 Александр Гамов
Александр ГамовЮнна Мориц: Держи удар, дистанцию и слово. Держи святую воду и перо. Держи картошки полное ведро…
— Юнна Петровна! Сейчас — всеобщий масочный режим и даже — всеобщая паника прослеживается от статистики по заболеванию COVIDом. Люди снова самоизолируются… — А я все время живу в уединении, без которого невозможно работать так, как я работаю. — Я сегодня — под впечатлением ваших стихов… Держи удар, дистанцию и слово… Держи картошки полное ведро…55 - Общество
 Венера Галеева
Венера ГалееваВторой кремцех. Книга учета петербургского крематория против официальной статистики
Когда в Петербурге официально сообщали о 3 умерших за сутки, в городском крематории сжигали 30 тел с пометкой COVID+. В распоряжении «Фонтанки» оказался документ, в котором по дням зафиксированы будни второго «коронавирусного» корпуса на Шафировском. Фото: Венера Галеева/«Фонтанка.ру» Судя по этим данным, пиковая смертность от новой инфекции в городе наблюдалась уже в мае — в…70 - Общество
 Алексей Аркадьевич
Алексей АркадьевичКогда мы себя угробим? Ядерный мусор Российской Федерации
Фото: Avrupahaberi.com Откуда берутся и куда пропадают самые опасные отходы в мире? И при чем здесь Чернобыль К сожалению, в мире сейчас всё больше и больше потребляется электроэнергии, и тенденции на уменьшение даже не предвидится. Только вот помимо безвредных для окружающей среды источников её генерации, таких как гидроэлектростанции, солнечные батареи, ветрогенераторы и других, в мире…43 - Общество
 Анатолий Круглов
Анатолий КругловБольшинство россиян не устраивает их зарплата
Большинство опрошенных жителей России заявило, что они хотели бы получать более высокую зарплату. Треть респондентов мечтает о росте уровня доходов сразу на 30-50%. 87% из более 4 тысяч опрошенных россиян в возрасте старше 18 лет сообщили, что их не устраивает размер их заработной платы. Таковы результаты исследования от сервиса «Работа.ру», которые публикует ТАСС. 15% респондентов хотели бы…18 - Общество
 По сообщениям информационных агентств
По сообщениям информационных агентствКатастрофа в Закавказье: геноцид армян
Фото отсюда Президент Нагорно-Карабахской Республики Араик Арутюнян обратился с экстренным обращением к армянскому народу. «Сегодня, в этот решающий исторический момент, когда турецко-азербайджанские и террористические банды напали на Арцах со всеми своими военными средствами с целью истребить или изгнать арцахских армян, тысячелетиями проживавших на своей родине, мы сражаемся насмерть во всех неравных условиях. Теперь они угрожают…47 - Общество
 Михаил Старков
Михаил СтарковКурганский губернатор рассчитывает на помощь военных врачей
Курганский губернатор Вадим Шумков на станции скорой помощи | Фото: kurganobl.ru В Курган прибыли военные медики из Центрального военного округа. 30 октября они встретились с губернатором и обсудили план действий. Курганские врачи заранее предупредили президента Владимира Путина, что своими силами региону не справиться с COVID-19. По данным Департамента здравоохранения Курганской области, в регионе начали работать 22…21
- Общество
 Екатерина Мищенко
Екатерина МищенкоЧем наc лечат: Авифавир
Быстрый, противовирусный, твой Что за молекула стоит за первым в мире специфическим препаратом от коронавируса, якобы разработанным в России, какие трудности перевода испытывают РНК-вирусы внутри клетки и можно ли верить заявлениям в СМИ в отсутствие научных публикаций в рецензируемых журналах, разбираемся в новом выпуске рубрики «Чем нас лечат». В отечественные клиники завозят первый зарегистрированный в…259 - Общество
 Екатерина Мищенко
Екатерина Мищенко«Средний возраст приборов подошел к критической черте»
Oliver Sved/Getty Images/Max Pixel/Indicator.Ru Как РАН лишили права голоса в заявках на обновление приборной базы и что с этим делать. Как надо обновлять научную инфраструктуру, каким организациям перечислят больше денег уже в этом году, почему Российскую академию наук отстранили от экспертизы в данном вопросе и помогут ли учтивые танцы выстроить плодотворное взаимодействие с Минобрнауки, читайте…49 - Общество
 Артем Космарский Екатерина Мищенко Яна Хлюстова
Артем Космарский Екатерина Мищенко Яна Хлюстова«По всему миру происходит инфляция оценок»
Члены Совета Проекта 5-100 — о современном высшем образовании С 24 по 26 октября в Москве прошло XII заседание Совета Проекта 5-100. Участие в нем приняли и иностранные участники. Indicator.Ru побеседовал с тремя из них о том, какими должны быть университеты, преподаватели и студенты — и насколько этому идеалу соответствуют российские вузы. Сэр Малколм Грант,…10.11.2019 1:05 62
Лента новостей
- Москва в выходные получит партию «Спутника V» для массовой вакцинации
- В России заканчиваются алмазы
- Новости экономики. 06.11.2020
- Китай закрывает границы с Россией из-за коронавируса
- Новости экономики. 05.11.2020
- Река Обь признана самой грязной в России
- Инвалиды вышли на акцию протеста в Минске
- Разные новости 05.11.2020
- Думе предложили расширить гарантии неприкосновенности экс-президентов
- Активисты сообщили о 17 задержанных на «Русском марше» в центре Москвы

